شعر
همچو سدیم از برای عشق ید پرپر شــدن چو ن کلر در سر هوای هاش مثبت داشتن
سخت ماندن در قبــال مشکلات زندگــــی نی چو الکانها هوای شعله در سر داشتن
دوستی با دیگران چون عنصر خوب نهـــم نی چو ارگون منزوی وگوaشه گیری داشتن
نیکنامی ونجابت چون گروه هشتمین همچو اهن درسر فکر مثبت داشتـــن
همچو همپوشانی سیگما که خیلی محکم است در رسیدن به هدف تصمیــــم راســــــخ داشتـــــن
قدرت اسیدها
قدرت اسيدها
چند تا عکس خوشگل واستون میذارم حالشو ببرین
۳تا عکس خوشگل در انتظارتونه برین ادامه مطلب ببینین چقدر شیمی قشنگه
الکل (2)
از میان روشهای صنعتی الکل میتوان راههای زیر را نام برد:
- آبدارکردن آلکنهای بدست آمده از کراکینگ نفت.
- فرایند السک از آلکنها، مونوکسید کربن و هیدروژن.
- تخمیر کربوهیدراتها
الکل (1)
آیا میدانید عاشق شدن یک فرایند شیمیایی است !!!
عامل ایجاد این تحریک، مولکول کوچکی موسوم به فنیل اتیل آمین است.این مولکول همراه با دوپامین و نور اپی نفرین میتواند یک حس نا معلوم ولی شادی آفرینی را که منجر به علاقه سیر ناپذیری می شود ایجاد کند.ولی متاسفانه در اینجا محدودیت هایی به خاطر برخی بمباران انتقال دهنده های عصبی ناشی از برخی پاسخ دهنده های کسل کننده وجود دارد.
فنیل اتیل آمین ماده ای شیمیایی طبیعی شبیه آمفتامین و دوپامین است که تجربه عالی عشق را برای ما فراهم می کند.
چیزی که توصیف عشق را مشکل می کند تلنگرهای اولیه آن در قشر جلوی مغزاست که انسان را قادر می سازد لذت بودن با شخصی خاص را ، حتی اگر تا آن زمان بک بار بیشتر او را ملاقات نکرده باشد ، برای خود پیش بینی کند. اگر این تلنگرها به اندازه کافی قوی باشند به آن (حافظه آینده) گویند که درگیر پاسخ به جنگ و گریزهای قدیمی قسمت جلوی مغز و مسئول رفتارهای ناخواسته ای چون لکنت زبان، عیاشی، لودگی و خنده های بلند به لطیفه های دیگران خواهد بود.اندورفینها که ساختاری شبیه به مرفین دارند بیشتر به ماده ای که می تواند در انسان احساس خوشی و شعف ایجاد کند شناخته شده اند. این مواد به عشاق ، آرامش مشابهی می بخشد ولی نه در همان لحظات اول.
اندورفینها در مراحل اولیه جذب با تحریک تک یاخته های خاصی در مغز میانی به شکل کاتالیزگر عمل کرده و آمفتامین های طبیعی قوی یعنی دوپامین و فنیل اتیل آمین را تحریک می کنند .آنها با فرمانهای خود در مغز فکر و خیال ها را طراحی می کنند ، هر فکرو خیالی را !!!!
مندلیف زیر و رو کننده ی علم شیمی
اورنیوم آینده ی جهان
ویژگی های فرمالدهید
ساختار های کربن
کربن

کربن به دوشکل بلوری الماس و گرافیت وجود دارد.خواص فیزیکی الماس وگرافیت به دلیل تفاوت در ساختار بلوری کاملا متفاوت است.
لکترونگاتیوی

تمایل نسبی یک اتم به جذب جفت الکترون های پیوندی دریک مولکول پایدار را الکترونگاتیوی گویند. راه های محاسبه الکترونگاتیوی که توسط پاولینگ انجام شد طبق معادله های زیر می باشد.
DAB = 1/2 ( DA-A+DB-B) + 23(XA-XB)2
و A = XA 125( الکترونخواهی - انرژی یونش )
که درآن X الکترونگاتیوی وD انرژی تفکیک پیوند می باشد .
دارورساني با استفاده از نقاط کوانتومي پوشيده شده با مولکول هاي شکر
گرافیت یا الماس؟
کربن به دوشکل بلوری الماس و گرافیت وجود دارد.خواص فیزیکی الماس وگرافیت به دلیل تفاوت در ساختار بلوری کاملا متفاوت است الماس فرم بلوری کربن باچگالی ( g/cm3 3/520) ٬ یک از سخت ترین ودیر گدازترین مواد شناخته شده است و....
کمی تا قسمتی طنز!
یا اعتراض در باب کمبود امکانات...
حالت پنجم ماده !!
پیوند هیدروژنی و نقش آن در زندگی
مقدمه
وقتی اتم هیدروژن به دو یا چند اتم دیگر پیوند شده باشد، یک پیوند هیدروژنی وجود دارد. این تعریف اشاره بر این دارد که پیوند هیدروژنی نمیتواند یک پیوند کووالانسی عادی باشد، زیرا اتم هیدروژن تنها یک اوربیتال (1S) در سطح انرژی به قدر کافی پایین دارد که درگیر تشکیل پیوند کووالانسی شود.جاذبه بین مولکولی و پیوند هیدروژنی
جاذبه بین مولکولی در برخی از ترکیبات هیدروژندار بطور غیر عادی قوی است. این جاذبه در ترکیباتی مشاهده میشود که در آنها بین هیدروژن و عناصری که اندازه کوچک و الکترونگاتیوی زیاد دارند، پیوند هیدروژنی وجود دارد. در این ترکیبات ، اتم عنصر الکترونگاتیو چنان جاذبه شدیدی بر الکترونهای پیوندی اعمال میکند که در نتیجه آن ، هیدروژن دارای بار مثبت قابل ملاحظه +δ میگردد. هیدروژن در این حالت ، تقریبا به صورت یک پروتون بیحفاظ است، زیرا این عنصر فاقد الکترون پوششی است. اتم هیدروژن یک مولکول و زوج الکترون غیر مشترک مولکول دیگر ، متقابلا همدیگر را جذب میکنند و پیوندی تشکیل میشود که به پیوند هیدروژنی مرسوم است. هر اتم هیدروژن قادر است تنها یک پیوند هیدروژنی تشکیل دهد.نقطه جوش و پیوند هیدروژنی
ترکیباتی که پیوند هیدروژنی دارند، خواص غیر عادی از خود نشان میدهند. تغییرات نقاط جوش در مجموعه ترکیبات SnH4 , GeH4 , SiH4 , CH4 مطابق روال پیش بینی شده برای ترکیبات است نیروهای بین مولکولی آنها منحصر به نبروهای لاندن است. نقطه جوش در این مجموعه با افزایش اندازه مولکولی ، زیاد میشود. ترکیبات هیدروژنی عناصر گروه چهار اصلی ، مولکولهای ناقطبی هستند. اتم مرکزی هر مولکول فاقد زوج الکترون غیر مشترک است. در گروههای پنج ، شش و هفت اصلی نیروهای دو قطبی - دوقطبی به نیروهای لاندن در چسباندن مولکولها به یکدیگر کمک میکند. ولی نقطه جوش نخستین عنصر هر مجموعه (NH3,H2O , HF) بطور غیر عادی بالاتر از نقاط جوش سایر اعضای آن مجموعه است. پیوند هیدروژنی در هر یک از این سه ترکیب ، جدا شدن مولکولها را از مایع مشکلتر میکند.جوان شدن با شیمی
● انتخاب بیمار
همانند تمامی اقدامات زیبایی صورت، در اینجا نیز انتخاب مناسب بیمار و برگزیدن درمان به خصوص برای هر شخص، برای كسب موفقیت بسیار مهم است. مهارت تكنیكی بدون توانایی انتخاب بیمار مناسب ممكن است منجر به نتایج فاجعه آمیزی شود . مواد شیمیایی لایه بردار نیز همانند تمامی روشهای بازسازی پوست صورت، موارد مصرف بالینی مشخص دارند . به طور كلی افراد دارای چروكهای خفیف صورت یا اختلالات رنگدانهای خفیف بهترین شرایط را برای استفاده از شیوه های بازسازی سطحی یا با عمق متوسط دارا هستند.
حرکت اسپینی الکترون
الکترون در اتم ، علاوه بر این که تحت تاثیر نیروی جاذبه هسته ، به دور آن میچرخد، دارای یک حرکت چرخشی به دور خود نیز میباشد. این نوع چرخش را اصطلاحا اسپین الکترون میگویند. «اسپین» واژه انگلیسی (Spin) است که به معنای چرخش میباشد.
مقدمه
میدانیم که کره زمین دارای دو نوع حرکت وضعی و انتقالی است. حرکت انتقالی آن به دور خورشید بوده و حرکت وضعی به دور خودش میباشد. هر یک از این دو نوع حرکت ، دارای اندازه حرکت زاویهای مخصوص به خود هستند که در مورد حرکت انتقالی ، اندازه حرکت زاویهای مداری و در مورد حرکت وضعی ، اندازه حرکت زاویهای اسپینی میگویند، بدیهی است که اندازه حرکت زاویهای کل برابر با مجموع این دو اندازه حرکت است.
اگر مدلی را در نظر بگیریم که زمین فقط یک نقطه مادی باشد، انتساب تکانه زاویهای به آن بیمعنی خواهد بود، اما در مدل دیگری که زمین را با ابعاد محدود در نظر میگیریم، وجود اندازه حرکت زاویهای اسپینی نیز امکان پذیر است. لذا اگر این قضیه را در مورد مدل اتمی بور بکار ببریم، با این فرض که الکترون یک بار نقطهای نبوده، بلکه یک کره کوچک فرض شود، در این صورت الکترون علاوه بر اندازه حرکت زاویهای مداری دارای اندازه حرکت زاویهای اسپینی نیز خواهد بود.
پنجمین شکل کربن
قویترین اسیدی که شناخته شد
یک کیلو آهن یا یک کیلو پنبه؟
این مفهوم علمی چیزی نیست مگر «چگالی» که اگر به کودکی خودتان رجوع یا به درس و مشق بچهتان توجه کنید، میبینید که در موقع یادگرفتناش سؤال و ابهام زیادی وجود دارد.
جدول تناوبی(شکلی جدید از جدول تناوبی در ذهن شما )
جدول تناوبی عناصر

اگرفهرست برنامه هابه شکل جدول باشد،می توانیدآنچه راکه می خواهید،بایک نگاه تشخیص دهید، تنظیم جدول روشی موثر برای نشان دادن مقدارزیادی اطلاعات مربوط به یکدیگر است.
پس از کشف عنصر هاوخواص آنها ،دانشمندان سعی کردند تا آنها را بر اساس نظم ویژه ای طبقه بندی کنند.
برای طبقه بندی عناصر به روش مدون ،کوشش های زیادی شد،ازجمله دسته بندی سه تایی دوبرینر، قانون اوکتاوهای نیولندز و جدول های مندلیف و میر را می توان نام برد .
مندلیف جدول تناوبی خودرابراساس جرم اتمی و خواص مشابه عناصرتنظیم کرد.ونتیجه گرفت که خواص عناصر تابعی از جرم اتمی آنهاست.
اما نواقص جدول مندلیف وکشف عدداتمی توسط موزلی نشان داد که خواص عناصر تابعی از عدداتمی عناصر است.جدول تناوبی جدید براساس عدداتمی مرتب گردید.
جدول تناوبی جدید ارتباط تشابه خواص عناصر را با آرایش الکترونی آن ها نشان می دهد و جایگاه عنصر درجدول ساختارالکترونی آن را مشخص می کند.
عناصری که دریک گروه و زیرهم چیده شده اند خواص مشابه وآرایش الکترونی لایه ظرفیت یکسان داشته ، ودرنتیجه خواص فیزیکی و شیمیایی مشابه وترکیبات نظیرهم دارند.
از دوره دوم ( تناوب ) جدول ، از چپ به راست ازخصلت فلزی عنصرها کاسته شده و بر خصلت نافلزی افزوده می شود ودرانتها ، دوره به یک گاز نجیب ختم می شود.
عناصر پرتو زا (رادیو اکتیو)
توریم و اورانیوم و بعضی از عناصر دیگر بدون هیچ اثر خارجی (یعنی به سبب عوامل داخلی) پیوسته تابش مرئی گسیل می دارند. این تابش مانند اشعه ایکس به درون حائل های کدر نفوذ می کند. و روی فیلمهای عکاسی اثر می گذارد. و اثر یونشی به وجود می آورد. ویژگی گسیل خود به خودی چنین تابش به پرتوزایی معروف است به عناصر دارای این ویژگی عناصر رادیو اکتیو می گویند و تابشی که این عناصر گسیل می دارند تابش پرتوزایی (تشعشع هسته ای) نامیده می شود. خاصیت پرتوزایی اورانیم را در سال 1896 آنتوان هانری بکرل فیزیکدان فرانسوی کشف کرد. پرتوزایی اندکی پس از کشف اشعه ایکس کشف شد.
عناصر رادیو اکتیو محصول آزمایشات اولیه
گسیل پرتوهای ایکس اولین بار در بمباران دیواره های شیشه ای لامپ تخلیه گازی با پرتوی کاتدی کشف شد. موثرترین نتیجه این بمباران تابانی شدید شیشه به رنگ سبز یعنی لیانی است. از اینجا معلوم می شود پرتوهای ایکس حاصل لیانی است و با هر لیانی همراهند، از جمله موردی که با نور برانگیخته شود.
اشعه ی کاتدی
اشعهي كاتدي چيست؟
جريان از اين قرار است كه در ساختار بلور فلزّات، به ازاي هر اتم يك يا چند الكترون آزاد وجود دارد كه تقريباً در همهي نمونهي فلزّي كه ميبينيم ميتواند آزادانه حركت كند. ميزان انرژي لازم براي اين كه بشود اين الكترونها را از فلز خارج كرد كم است و البتّه براي فلزّات مختلف متفاوت است. امّا به طور كلّي اگر شما يك قطعه فلز را داغ كنيد، ميلياردها الكترون به راحتي انرژي لازم براي فرار كردن از ساختار بلوري فلز را به دست ميآورند و از سطح آن جدا ميشوند.
فلزّاتي كه انرژي لازم براي جدا كردن الكترون از آنها كمتر است، غالباً براي ساخت كاتد به كار ميروند و جرياني كه با گرم كردن آنها (كاتد گرم) يا انرژي دادن به آنها به روشهاي ديگر (كاتد سرد) به دست ميآيد، جريان يا اشعهي كاتدي نام دارد.
ساختار هسته
ذرات زیر اتمی
ذراتی که اتم را تشکيل می دهند ذرات زير اتمی می نامند.اين ذرات به دو گروه بزرگ تقسيم می شوند.
۱- لیپتونها: که الکترون مشهورترين آنها می باشد
واقعا ذرات بنيادی هستند.
۲ـ هادرونها: هادرونها که ذرات کوچکتر ولی سنگينتراز لیپتونها می باشند ، شامل:
ـ باريونها: متداولترين باريون همان پروتونها و نوترونها هستند.
پروتونها و نوترونها بانيروی هسته ای درکنار يکديگر در حجم کوچک هسته قرار می گيرند .
ـ مزون: مهمترين مزونها پيونها و کيونها می باشند.
ذراتی که درهسته اتم جای می گيرند نوکلئون می ناميم .
شیمی و پزشکی
یون
ترکیبات یونی متشکل از تعداد زیادی آنیون و کاتیون هستند که با طرح معین هندسی در کنار هم قرار گرفتهاند و یک بلور بوجود میآورند. هر بلور ، به سبب جاذبههای منفی ـ مثبت یونها به هم ، نگهداشته شده است. فرمول شیمیایی یک ترکیب یونی نشانه سادهترین نسبت یونهای مختلف برای به وجود آوردن بلوری است که از نظر الکتریکی خنثی باشد.
پیوند یونی IonicBond
|
پیوند یونی جاذبهای است که بین یونهای مثبت و منفی وجود دارد و آنها را در یک ساختار بلوری به هم نگه میدارد. این پیوند ناشی از انتقال الکترون بین اتم هاست. |
ماهیت یون
وقتی اتمها به یون تبدیل میشوند، خواص آنها شدیدا تغییرمیکند. مثلا مجموعهای از مولکولهای برم قرمز است. اما یونهای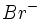 در رنگ بلورماده مرکب هیچ دخالتی ندارند. یک قطعه سدیم شامل اتمهای سدیم نرم است. خواص فلزی دارد و بر آب به شدت اثر میکند. اما یونهای آن در آب پایدارند.
در رنگ بلورماده مرکب هیچ دخالتی ندارند. یک قطعه سدیم شامل اتمهای سدیم نرم است. خواص فلزی دارد و بر آب به شدت اثر میکند. اما یونهای آن در آب پایدارند.
مجموعه بزرگی از مولکولهای کلر ، گازی سمّی بهرنگ زرد مایل به سبز است، ولی یونهای کلرید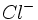 مواد مرکب رنگ ایجاد نمیکنند و سمّی نیستند. به همین لحاظ است که یونهای سدیم و کلر را به صورت نمک طعام میتوان بدون ترس از واکنش شدید روی گوجه فرنگی ریخت. وقتی اتمها به صورت یون در میآیند، ماهیت آنها آشکارا تغییر میکند.
مواد مرکب رنگ ایجاد نمیکنند و سمّی نیستند. به همین لحاظ است که یونهای سدیم و کلر را به صورت نمک طعام میتوان بدون ترس از واکنش شدید روی گوجه فرنگی ریخت. وقتی اتمها به صورت یون در میآیند، ماهیت آنها آشکارا تغییر میکند.